
Entre el 7 y el 8% de las bacterias ya son resistentes a los fármacos
El número se triplicó tras la pandemia. Especialistas advierten que es indispensable un uso adecuado de los antimicrobianos, también en la cría de animales para consumo y buenos sistemas de vigilancia.
En agosto del año pasado, un centro médico privado de la Ciudad Autónoma de Buenos Aires entró en emergencia: uno de sus pacientes trasplantados presentaba una infección urinaria que no cedía ante ninguna medicación. A ese caso le siguieron siete más en lo que constituyó el primer brote registrado en el país de una bacteria resistente a los 30 antibióticos disponibles (había habido uno en 2016, pero no se contaba con ese número de fármacos), la Klebsiella pneumoniae.
“Desde entonces estamos luchando. Desaparece por momentos, parece que está controlado, pero es muy difícil evaluar todos los reservorios o a veces son los pacientes los que ingresan con la bacteria –explica Fernando Pasteran, investigador del Laboratorio Nacional y Regional de Referencia en Antimicrobianos Anlis-Malbrán–. Es la manifestación más cruda y más dura de la crisis de la resistencia a los antibióticos. No poder ofrecerles un tratamiento a estos pacientes. Estimamos que se va a resolver y que no perdurará en el tiempo, pero estos episodios van a ser cada vez más frecuentes”.
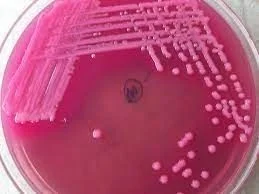
Placa con bacterias resistentes a los antibióticos
Esto, precisamente, es lo que inquieta y moviliza a los sistemas sanitarios del mundo. Un estudio realizado por la Organización Mundial de la Salud (OMS) en 87 países reveló que en todos estaba creciendo la resistencia a los antimicrobianos. “Se avecina una ‘tormenta perfecta’ –comenta Pasteran–. Los microbios mutan muy rápido, dejan de ser sensibles a sus efectos, y cada vez se desarrollan menos de este tipo de drogas. Si no se detiene este proceso, en un par de décadas podrían llegar a ser riesgosos procedimientos habituales como las extracciones dentales o las cesáreas”.
Una señal inquietante del problema es que cada vez hay más bacterias que sólo responden a una o dos drogas. Se las conoce como “extremadamente resistentes”. “Después de la pandemia, entre un 7 y un 8% entran dentro de esta categoría –destaca el científico–. En la Argentina, el Covid potenció los problemas preexistentes y aumentó la resistencia a los antimicrobianos. El hecho de que al comienzo se tratara a todos los pacientes con antibióticos es una de las causas por las que aumentamos las infecciones por bacterias resistentes. Desde el Malbrán mostramos que las ‘superbacterias’ pasaron de un 20 a un 30% en un año, o sea, hicieron un salto que normalmente llevaba diez, ya que aumentan uno o 2% anual. En este momento, las dos entidades bacterianas que causan las infecciones intrahospitalarias más difíciles de tratar (las enterobacterias resistentes a carbapenemes y las del género Acinetobacter) aumentaron la carga de enfermedad casi tres veces, un 300%”.

(GRÁFICO: ANLIS-MALBRÁN)
Un mapa desigual
Hace unos días, se realizó en Buenos Aires el cuarto encuentro de la Red de Centros Colaboradores de la OMS para la Evaluación de Calidad y Vigilancia de la Resistencia a los Antimicrobianos (RAM), con la presencia de expertos locales e internacionales. Durante una conferencia de prensa tras la apertura del evento, Kitty van Weezenbeek, directora de Vigilancia, Prevención y Control de la Resistencia Antimicrobiana de la OMS, explicó que si bien en la actualidad no hay faltantes, el ritmo de lanzamiento de nuevos fármacos contra las infecciones multirresistentes es muy lento: “Desarrollarlos lleva 10 o 15 años, y para la mayoría de las compañías no es buen negocio, porque se usan durante algunos días o un par de semanas, en comparación con los de enfermedades crónicas, que deben administrarse a lo largo de décadas”.
Y agregó: “muchos piensan que si les prescriben antibióticos de amplio espectro, es mejor, pero eso termina causando más resistencia a fármacos. El problema es que numerosos países carecen de los servicios de laboratorio necesarios para hacer la caracterización de las infecciones”. Van Weezenbeek también destacó que la Argentina posee un sistema de vigilancia que se encuentra entre los mejores del mundo.
Escherichia coli
“Yo trabajo en el Instituto hace 27 años y hay toda una tradición –cuenta Pasteran–. En ese entonces, ya existía el problema de las bacterias resistentes, pero era incipiente. Recién se empezaban a comprometer las ‘cefalosporinas de espectro extendido’. No era un problema prioritario porque la industria farmacéutica competía por el desarrollo de antibióticos. Teníamos esa tranquilidad. Si aparecía resistencia a alguna droga, sabíamos que teníamos todavía un arsenal para combatirla. Pero con la prolongación de la expectativa de vida, las nuevas terapias para mejorar la salud humana (como los trasplantes o el tratamiento del cáncer) llevaron a un mayor número de cirugías, hospitalizaciones y, como consecuencia, más uso de antibióticos. Como las bacterias mutan mucho, la presión de selección condujo a microbios cada vez más resistentes y menos opciones de tratamiento. Y así llegamos a la crisis”.
Durante la pandemia, la gran cantidad de pacientes internados en terapia intensiva en poco tiempo más la desatención de los programas de control de infecciones, porque todo el sistema de salud estaba volcado a un único patógeno, el SARS-CoV-2, llevó a una “explosión” de bacterias resistentes. “Sobre todo, enterobacterias que tienen un mecanismo llamado NDM –detalla Pasteran–. Eso nos hace tener que utilizar antibióticos de última línea, de altísimo costo. No solo encarecen el gasto en salud, sino que dependemos de dos o tres moléculas”.
Cabe aclarar que el mapa no es uniforme en todo el país, ya que hay provincias con menores tasas de resistencia, como San Juan, Tierra del Fuego, La Pampa o Jujuy. “San Juan, por ejemplo, tiene una ley provincial y programas para controlarla desde hace diez años –cuenta el investigador–. Allí capacitaron a los inspectores municipales (cuya tarea habitual es controlar el tránsito), para que auditen las farmacias y corroboren que no se expendan antibióticos sin prescripción”.

En ese sentido, la Ley 27.680 de Prevención y Control de la Resistencia a los Antimicrobianos, aprobada por unanimidad el año pasado, llega en un momento en que es muy necesaria para que se activen los programas de uso optimizado y de control de infecciones en los hospitales, se reduzca el uso de antibióticos en la cría de animales de consumo y se fortalezca la vigilancia. En la Argentina, desde 1996, ese sistema lo integran hospitales de las 24 jurisdicciones. En un principio, fue una iniciativa liderada por el Malbrán y de la que participaban hospitales amigos. Ahora son las jurisdicciones las que eligen los “hospitales centinelas”.
La detección
“La vigilancia es muy laboriosa para el laboratorio de microbiología, porque utilizamos los mismos protocolos en todos los hospitales –enfatiza Pasteran–. Todos los años se hace un consenso de los antibióticos que se deben probar para cada entidad [bacteria] que vigilamos, y se utiliza un software de la Organización Mundial de la Salud para recabar los datos. El registro es nominal: paciente por paciente. Cada vez que se hace un antibiograma [una prueba de sensibilidad a antibióticos] se ingresa en este sistema, con lo que se reúnen entre 300.000 y 350.000 datos por año. Lleva mucho tiempo. A veces se necesitan pruebas adicionales a modo de confirmación. Muchas de ellas las desarrollamos y las validamos acá para que sean simples y económicas. También hay que cargar esa información adicional. El ‘consolidado’ se va analizando cada seis meses. Durante dos o tres semanas, ocho personas del Laboratorio de Referencia depuramos la base de datos para que se hagan los análisis. Todo germen que crece y al que se le hace un antibiograma se registra en el software y se manda a analizar. Tenemos datos de todo, todo, todo”.
Gracias a la tarea rápida y coordinada del Instituto Malbrán, los funcionarios del Ministerio de Salud y los equipos del centro médico donde se produjo el brote, los ocho pacientes que se infectaron con Klebsiella resistente a todos los antibióticos disponibles pudieron ser rescatados. “Hasta encontramos un mecanismo de resistencia que no estaba descripto –destaca Pasteran–. Las Klebsiellas tienen una enzima en su genoma que lo único que hace es conferir resistencia a la ampicilina. La presión de selección hizo que esta enzima cromosómica adquiriera cuatro mutaciones en su gen estructural y terminó afectando las drogas de última línea, que se lanzaron hace muy poquito en el país, algo que hasta ahora no había ocurrido. Nunca una bacteria se había vuelto resistente simultáneamente a todo. Se lo contamos a Robert Bonomo, investigador del Centro de Educación y Clínica de Investigación Geriátrica de Cleveland, Estados Unidos, que descubrió esta enzima hace 40 años y nos mandó un paper suyo en el que en un párrafo decía que su temor era que pasara esto. Y finalmente ocurrió. Es difícil saber en qué momento fue; creemos que esta mutación puede haber ocurrido en personas. La colonización podría haber ocurrido por abril o mayo [del año pasado], pero quedó solapada porque todavía tenía sensibilidad a otros antibióticos. Pero necesitamos más estudios”.
Acinetobacter baumannii
Para tratar a los pacientes afectados tuvieron que utilizar una combinación de tres antibióticos. El problema es que cada brote de pan-drogo-resistencia exige una combinación distinta que no se conoce a priori. “Por suerte, algo que nos dejó de positivo la pandemia es que ahora disponemos de otro tipo de tecnología –cuenta el especialista–. Pudimos hacer la secuenciación masiva del genoma de las bacterias involucradas y con esa información elegir en forma más criteriosa los antibióticos que podrían funcionar. En menos de dos semanas ya los teníamos [a diferencia de lo que sucedió en 2016, cuando se tardó alrededor de un mes y medio]”.
Para Llopis, de OPS Argentina, “La resistencia a los antimicrobianos es uno de los principales retos para la salud pública global. Tiene impacto en la salud humana, pero también en la producción animal y agrícola, y en el ambiente”. En la raíz del problema también está el uso extendido de estos fármacos como promotores del crecimiento en la producción animal, que ya están prohibidos en varios países.
Según las últimas estimaciones surgidas de 204 países y territorios hasta 2019, ese año se produjeron 1.27 millones de muertes directamente atribuibles a la resistencia bacteriana. África registra la tasa más alta (con 27,3 muertes por cada 100.000 habitantes) y Australasia, la menor (con 6,5 por 100.000). Se calcula que cada tres minutos muere un chico en el mundo por infecciones resistentes. Los seis principales patógenos involucrados fueron Escherichia coli, Staphylococcus aureus, Klebsiella pneumoniae, Streptococcus pneumoniae, Acinetobacter baumannii, y Pseudomonas aeruginosa.
“Esto no se puede mirar desde un punto de vista punitivo –concluye Pasteran–. Cuando ocurren estas cosas, que le pueden pasar a cualquiera, no es que alguien está haciendo algo mal. Son décadas y décadas de distintos actores que no revirtieron la situación”.
Por: NORA BÄR
© Copyright 2020-Radio Bicentenario 98.3 . Design by: Futurisi






